Karina Toledo | Agência FAPESP – Um tratamento inovador contra o câncer, feito com células reprogramadas do próprio paciente, foi testado pela primeira vez na América Latina por pesquisadores do Centro de Terapia Celular (CTC) da Universidade de São Paulo (USP) em Ribeirão Preto – um Centro de Pesquisa, Inovação e Difusão (CEPID) apoiado pela FAPESP.
Conhecida como terapia de células CAR-T, a técnica foi usada para tratar um caso avançado de linfoma difuso de grandes células B – o tipo mais comum de linfoma não Hodgkin, doença que afeta as células do sistema linfático. O paciente, de 63 anos, já havia sido submetido sem sucesso a várias linhas diferentes de quimioterapia desde 2017.
“A expectativa de sobrevida desse paciente era menor que um ano. Para casos como esse, no Brasil, normalmente restam apenas os cuidados paliativos. Contudo, menos de um mês após a infusão das células CAR-T observamos melhora clínica evidente e até conseguimos eliminar os remédios para dor”, contou Renato Cunha, pesquisador associado ao CTC e coordenador do Serviço de Transplante de Medula Óssea e Terapia Celular do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto (HC-FMRP-USP).
A terapia de células CAR-T (acrônimo em inglês para receptor de antígeno quimérico) foi inicialmente desenvolvida nos Estados Unidos, onde é oferecida por dois laboratórios farmacêuticos a um custo de US$ 400 mil – sem considerar os gastos com internação. Já a metodologia desenvolvida no CTC tem custo aproximado de R$ 150 mil, que pode se tornar ainda mais baixo se o tratamento passar a ser oferecido em larga escala.
“Trata-se de uma tecnologia muito recente e de uma conquista que coloca o Brasil em igualdade com países desenvolvidos. É um trabalho de grande importância social e econômica para o país”, afirmou Dimas Tadeu Covas, coordenador do CTC e do Instituto Nacional de Ciência e Tecnologia em Células-Tronco e Terapia Celular, apoiado pela FAPESP e pelo Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
O primeiro paciente foi atendido pela equipe do CTC e do Hemocentro do HC-FMRP-USP na modalidade de tratamento compassivo, que permite o uso de terapias ainda não aprovadas no país em casos graves sem outra opção disponível. O grupo pretende agora iniciar um protocolo de pesquisa com um número maior de voluntários. “Já temos outros dois pacientes com linfomas de alto grau em vias de receber a infusão de células reprogramadas”, contou Cunha.
Como funciona
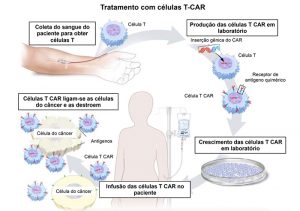
A partir de amostras de sangue dos pacientes a serem tratados, os pesquisadores isolam um tipo de leucócito conhecido como linfócito T, um dos principais responsáveis pela defesa do organismo graças à sua capacidade de reconhecer antígenos existentes na superfície celular de patógenos ou de tumores e desencadear a produção de anticorpos.
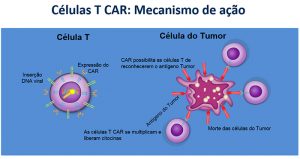
Com auxílio de um vetor viral (um vírus cujo material genético é alterado em laboratório), um novo gene é introduzido no núcleo do linfócito T, que então passa a expressar em sua superfície um receptor (uma proteína) capaz de reconhecer o antígeno específico do tumor a ser combatido.
“Ele é chamado de receptor quimérico porque é misto. Parte de um receptor que já existe no linfócito é conectada a um receptor novo, que é parte de um anticorpo capaz de reconhecer o antígeno CD19 [antiCD-19]. Com essa modificação, os linfócitos T são redirecionados para reconhecer e atacar as células tumorais”, explicou Cunha.
Os leucócitos reprogramados são “expandidos” em laboratório (colocados em meio de cultura para que se proliferem) e depois infundidos no paciente. Antes do tratamento, uma leve quimioterapia é administrada para preparar o organismo.
“Cerca de 24 horas após a infusão das células CAR-T tem início uma reação inflamatória, sinal de que os linfócitos modificados estão se reproduzindo e induzindo a liberação de substâncias pró-inflamatórias para eliminar o tumor. Além de febre, pode haver queda acentuada da pressão arterial [choque inflamatório] e necessidade de internação em Unidade de Terapia Intensiva [UTI]. O médico deve ter experiência com a técnica e monitorar o paciente continuamente”, disse.
O aposentado submetido ao protocolo no HC da FMRP-USP no dia 9 de setembro já superou a fase crítica do tratamento, conseguiu se livrar da morfina – antes usada em dose máxima – e não apresenta mais linfonodos aumentados no pescoço.
“Além desses sinais clínicos de melhora, conseguimos detectar as células CAR-T em seu sangue e essa é a maior prova de que a metodologia funcionou”, disse Cunha.
De acordo com o pesquisador, somente após três meses será possível avaliar com mais clareza se a resposta à terapia foi total ou parcial – algo que depende do perfil biológico do tumor. Os linfócitos reprogramados podem permanecer no organismo pelo resto da vida, mas também podem desaparecer após alguns anos.
Versão brasileira
O projeto que possibilitou a produção das células CAR-T teve início há cerca de quatro anos, quando foi renovado o apoio da FAPESP ao CTC. Nesse período, foram conduzidos estudos fundamentais sobre as construções virais mais usadas para a modificação gênica, bem como estabelecidos modelos animais para os estudos pré-clínicos. Cerca de 20 pesquisadores, incluindo médicos e biólogos celulares e moleculares, além de engenheiros especializados em cultivo celular em larga escala, participam do projeto.
Mais recentemente, Cunha se incorporou ao time com a experiência clínica e laboratorial adquirida durante estágio realizado no National Cancer Institute, centro ligado aos National Institutes of Health (NIH) dos Estados Unidos e pioneiro na técnica. Em dezembro de 2018, o pesquisador recebeu da Associação Americana de Hematologia (ASH, na sigla em inglês) o ASH Research Award e uma bolsa de US$ 150 mil para contribuir com o desenvolvimento da técnica na FMRP-USP. O projeto, no seu conjunto, teve apoio financeiro, além da FAPESP e do CNPq, do Banco Nacional de Desenvolvimento Econômico e Social (BNDES), da Financiadora de Inovação e Pesquisa (Finep), da Secretaria de Estado da Saúde de São Paulo e do Ministério da Saúde.
“A metodologia que desenvolvemos é específica para o tratamento de linfoma, mas a mesma lógica pode ser usada para qualquer tipo de câncer. Estamos trabalhando em protocolos para o tratamento de leucemia mieloide aguda e para mieloma múltiplo. Também estamos acertando uma parceria com uma universidade japonesa com foco em tumores sólidos, como o de pâncreas”, contou Rodrigo Calado, professor da FMRP-USP e membro do CTC.
O objetivo do grupo, segundo Calado, é desenvolver tratamentos de custo acessível a países de renda média e baixa e possíveis de serem incluídos no rol de procedimentos do Sistema Único de Saúde (SUS).
“O custo da terapia de células CAR-T é muito próximo do valor que o SUS repassa para um transplante de medula óssea – hoje em torno de R$ 110 mil. Então o tratamento pode ser considerado acessível”, disse Calado.
Covas lembrou que o CTC tem tradição em terapias pioneiras, entre elas a aplicação de células mesenquimais para tratamento de diabetes e o transplante de medula óssea em portadores de anemia falciforme.
“Só conseguimos desenvolver o protocolo CAR-T de modo relativamente rápido porque temos uma estrutura há muito tempo em construção. Esse investimento da FAPESP em ciência básica, em formação de pessoas e em infraestrutura de pesquisa agora se traduz em novos tratamentos mais eficazes contra o câncer”, disse o coordenador do CTC.